Фармакокинетика (ФК) антимикробных препаратов
Share this step
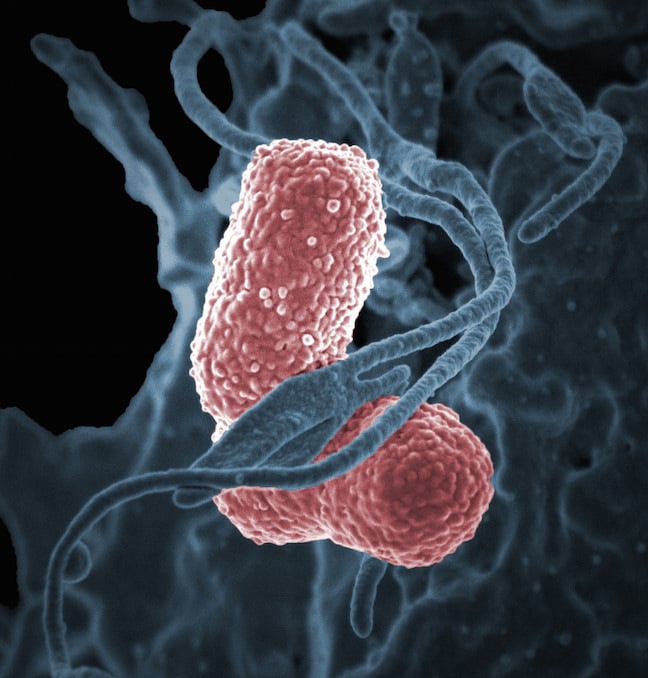
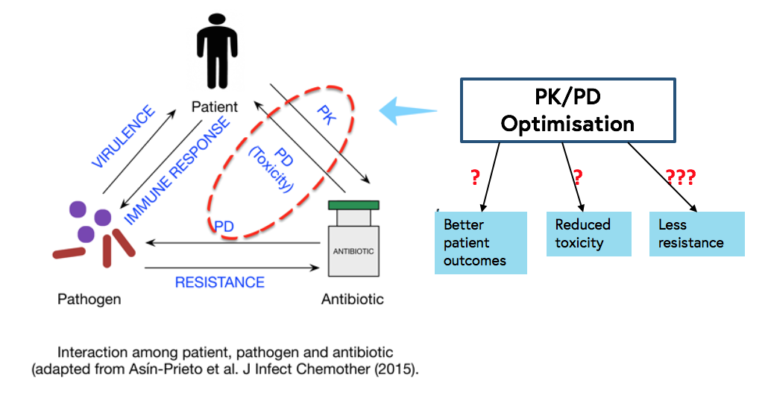
Исход бактериальной инфекции определяются многими факторами, на большинство из которых врачи не могут оказывать влияние:
- вирулентностью микроорганизма и устойчивостью к антибиотикам
- иммунным ответом макроорганизма
- фармакодинамическими (ФД) свойствами антибиотика.
Единственным фактором, который в некоторой степени может быть модифицирован медицинской организацией, является фармакокинетика (ФК) антимикробных препаратов.
ФК определяется как
«закономерности взаимодействия препарата и организма: всасывания, распределения, метаболизма и выведения (словарь Merriam-Webster), или проще говоря, «то, что организм делает с лекарством», в отличие от фармакодинамики, которая определяется как «то, что лекарство делает с организмом». Хотя мы не можем влиять на метаболизм конкретного лекарственного препарата, мы можем влиять на то, как мы вводим препарат (способ применения, время суток, доза, частота и скорость введения).
На метаболизм конкретного лекарственного препарата повлиять невозможно, но можно контролировать способ его применения (путь введения, время суток, доза, частота и скорость введения).
Для оптимизации ФК/ФД антибиотиков, необходимы хорошие базовые знания о ФК/ФД параметрах у разных групп пациентов. Важно помнить, что ФК/ФД параметры конкретного лекарственного средства могут различаться у новорожденных, детей, пожилых людей, больных с тяжелой формой заболевания, страдающих ожирением, пациентов с заместительной почечной терапией, разных этнических групп, разных полов и у пациентов с особыми заболеваниями, такими как муковисцидоз, поскольку всасывание, распределение, метаболизм и выведение лекарственных веществ у них могут варьировать.
К сожалению, для многочисленных «старых» антимикробных препаратов детальная характеристика ФК/ФД параметров отсутствует, поскольку они выводились на рынок в то время, когда такие данные не требовались для выдачи разрешения регулирующими органами, а технические возможности были ограниченными (например, в отношении точного измерения уровней лекарственных препаратов и компьютерного моделирования ФК/ФД). Кроме того, ФК/ФД параметры могут быть описаны только для конкретных популяций (например, здоровых добровольцев) и, таким образом, их трудно экстраполировать на другие популяции.
Задачу оптимизации ФК/ФД параметров значительно облегчает проведение терапевтического лекарственного мониторинга (ТЛМ) – то есть определение концентрации лекарственного средства в жидкостях организма (как правило, в крови), доступное в настоящее время для многих антимикробных препаратов, поскольку даже в пределах конкретной популяции пациентов существуют значительные индивидуальные вариации ФК.
Влияние антибиотиков на бактерии, то есть гибель микроорганизмов или ингибирование их роста, можно в основном описать тремя ФК/ФД индексами, которые устанавливают взаимосвязь между фармакокинетическими и микробиологическими параметрами:
• Время, в течение которого (свободная) концентрация антибиотика в очаге инфекции выше, чем минимальная подавляющая концентрация (МПК); сокращенно обозначается как «время выше МПК» или просто «T > МПК»
• Отношение (свободной) пиковой концентрации антибиотика (Cmax) в очаге инфекции к минимальной подавляющей концентрации (МПК): Cmax/МПК
• Отношение «площади под фармакокинетической кривой (концентрация-время)» (AUC) в течение 24 часов к МПК (AUC0-24/МПК).
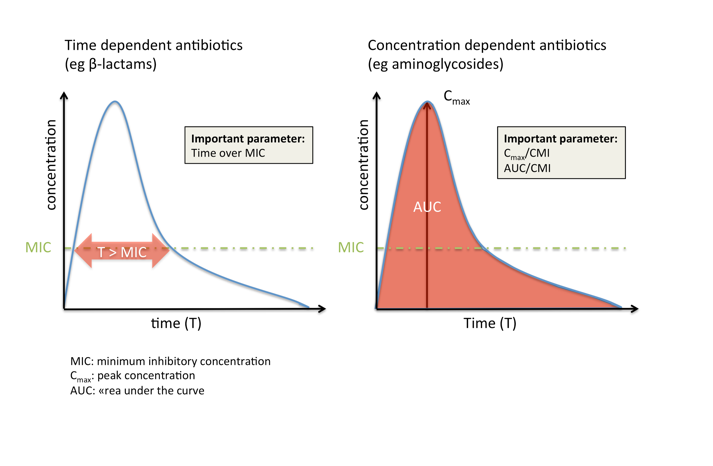
Ориентировочно антибиотики могут быть классифицированы на основе выбора ФК/ФД индекса, который наилучшим образом прогнозирует их эффективность:
• Времязависимые антибиотики, например, β-лактамы, эффективность которых зависит от длительности поддержания концентрации (не менее 50–60% интервала дозирования для β-лактамов) на уровне выше МПК. Увеличение концентрации c четырехкратного до пятикратного превышения МПК, обычно не влияет на эффективность, но может увеличить токсичность (например, вызвать судороги).
• Напротив, эффективность концентрационнозависимых антибиотиков, например, аминогликозидов, зависит от того, насколько их концентрация в очаге инфекции превышает МПК, тогда как время, в течение которого сохраняется эта концентрация, менее существенно.
• Многие классы антибиотиков (например, гликопептиды и фторхинолоны) попадают в третью категорию, где эффективность зависит как от концентрации, так и от времени.
Хотя эти принципы теоретически применимы ко всем лекарственным средствам, оптимизация ФК/ФД параметров в наибольшей степени используется в клинической практике в отношении β-лактамов и аминогликозидов.
Непрерывная или продленная инфузия β-лактамов
Учитывая упомянутые выше принципы, в настоящее время многие специалисты являются сторонниками введения β-лактамных антибиотиков путем продленных (более одного часа, но менее 24 часов) или непрерывных инфузий, для максимального повышения индекса T > МПК.
При осуществлении такого подхода для обеспечения быстрого достижения целевых параметров необходимо вводить нагрузочную (ударную) дозу (иначе может потребоваться много времени для достижения необходимой целевой концентрации).
Кроме того, необходимо учитывать стабильность антибиотика. Некоторые препараты при комнатной температуре стабильны в течение 24 часов (например, пиперациллин-тазобактам), другие – только в течение 3–4 часов (например, имипенем), и требуют либо частых смен инфузионного раствора (при непрерывной инфузии), либо введения в виде продленной инфузии (а не непрерывной).
Также необходимо учитывать лекарственные взаимодействия с другими назначаемыми внутривенно препаратами и некоторые практические проблемы (мобильность пациентов, количество возможных сосудистых доступов). Хотя концепция непрерывной или продленной инфузии β-лактамов (в сочетании с ТЛМ) привлекательна и основана на прочной теоретической базе, следует упомянуть, что клинических доказательств того, что оптимизация ФК/ФД приводит к улучшению результатов лечения пациентов, по-прежнему недостаточно. Можно предположить, что преимущества оптимизации ФК/ФД, в первую очередь, относятся к инфекциям, вызванным микроорганизмами, с относительно высокими значениями МПК β-лактамов (например, Pseudomonas aeruginosa, энтеробактерии, продуцирующие карбапенемазы и т. д.).
Недавнее многоцентровое рандомизированное контролируемое исследование, в котором сравнивались непрерывный и прерывистый режимы введение β-лактамного антибиотика у пациентов с тяжелым сепсисом, не показало преимуществ непрерывной инфузии по таким параметрам, как количество дней жизни без интенсивной терапии на 28-й день, смертности на 90-й день, клинического выздоровления через 14 дней после прекращения антибиотикотерапии, дней жизни без органной недостаточности на 14-й день и продолжительности бактериемии. Далханти и др. (Dulhunty et al.)
Кроме того, наблюдается некоторый скептицизм в отношении существенного влияния этого подхода на контроль резистентности к антибиотикам. Тем не менее, учитывая минимальные недостатки, непрерывная или продленная инфузия β-лактамов стала стандартом оказания помощи в некоторых центрах, и, надеюсь, скоро появятся доказательства ее полезности.
Аминогликозиды
ТЛМ для этого класса лекарственных препаратов давно стал обычной клинической практикой во многих центрах, главным образом с целью снижения токсичности (в основном нефро- и ототоксичности).
Аминогликозиды являются классическим примером концентрационно-зависимых антибиотиков с Cmax/МПК (с оптимальной эффективностью >8–10) в качестве наиболее важного показателя ФК/ФД, что делает введение этого класса лекарств один раз в сутки логичным выбором.
Кроме того, этот способ введения может также снизить вероятность развития нефротоксичности. Остается некоторая неопределенность в отношении оптимального способа введения, в тех случаях, когда необходимо обеспечить синергизм с β-лактамными антибиотиками в отношении грамположительных бактерий, например, для лечения энтерококкового эндокардита (так, например, американские и европейские рекомендации по ведению пациентов с эндокардитами 2015 года расходятся во мнениях по этому вопросу).
Основываясь на результатах исследований, выполненных на животных моделях, по-прежнему рекомендуется многократное ежедневное дозирование аминогликозидов, хотя в настоящее время руководства часто рекомендуют двукратное введение в течение суток вместо трехкратного, а некоторые руководства даже высказываются за однократное введение даже для инфекций, вызванных грамположительными патогенами. Если используется однократное введение в течение суток, пиковые уровни не нужно контролировать, так как высокая доза обеспечивает достаточные пиковые концентрации. Рекомендуется мониторировать только минимальные остаточные концентрации препарата, чтобы исключить его накопление и, следовательно, потенциальную токсичность.
Share this
Стратегия контроля антимикробной терапии (СКАТ): контроль антибиотикорезистентности

Стратегия контроля антимикробной терапии (СКАТ): контроль антибиотикорезистентности


Reach your personal and professional goals
Unlock access to hundreds of expert online courses and degrees from top universities and educators to gain accredited qualifications and professional CV-building certificates.
Join over 18 million learners to launch, switch or build upon your career, all at your own pace, across a wide range of topic areas.
Register to receive updates
-
Create an account to receive our newsletter, course recommendations and promotions.
Register for free







